Glutamát (neurotranszmitter): meghatározás és funkciók
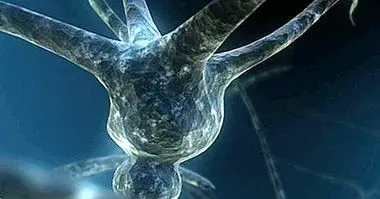
az glutamát közvetíti a központi idegrendszer (CNS) legtöbb izgatottsági szinapszáját. Ez az érzékszervi, motoros, kognitív, érzelmi információ fő közvetítője, és az emlékezet kialakulásában és helyreállításában az agy szinapszisainak 80-90% -ában van jelen.
Abban az esetben, ha mindez kevés érdeme, a neuroplasztikában, a tanulási folyamatokban is beavatkozik, és a GABA - a CNS fő gátló neurotranszmittere - előfutára. Mi mást kérhet egy molekula?
Mi a glutamát?
valószínű egyike volt az idegrendszer legelterjedtebb neurotranszmittereinek . Az utóbbi években tanulmánya nőtt a különböző neurodegeneratív patológiákkal (például az Alzheimer-kórral) való kapcsolatának köszönhetően, amely számos betegségben erős farmakológiai célt tűzött ki.
Azt is meg kell említeni, hogy receptorainak összetettsége miatt ez az egyik legkomplikáltabb neurotranszmitter, amelyet tanulmányozni kell.
A szintézis folyamata
A glutamát szintézisének folyamata a Krebs ciklusban vagy a trikarbonsavak ciklusában kezdődik. A Krebs-ciklus anyagcsere út vagy, hogy megértsük, a kémiai reakciók egymást követő szakaszában, hogy a mitokondriumban sejtes légzés jöhessen létre . Az anyagcsere ciklus úgy értelmezhető, mint egy óra mechanizmusa, amelyben mindegyik felszerelés teljesíti a funkciót, és egy darab egyszerű meghibásodása miatt az óra elrontja vagy nem jelölheti meg az időt. A biokémia ciklusai ugyanazok. Egy molekula folyamatos enzimatikus reakciókkal - órás fogaskerekekkel - megváltoztatja formáját és összetételét azzal a céllal, hogy sejtes funkciót eredményezzen. A glutamát fő prekurzora az alfa-ketoglutarát, amely aminocsoportot kap transzaminálással glutamátvá.
Érdemes megemlíteni egy másik, igen jelentős prekurzor: glutamin. Amikor a sejt felszabadítja a glutamátot az extracelluláris térbe, az asztrociták - egyfajta gliasejtek - visszanyerik ezt a glutamátot, amely egy glutamin szintetáz enzim révén glutaminná válik. akkor, az asztrociták felszabadítják a glutamint, amelyet a neuronok újra visszaadják glutamátba . És valószínűleg több is kérni fogja a következőket: És ha vissza kell adniuk a glutamint a glutamátba az neuronban, miért gátolja az asztrocitát a glutamin szegény glutamátgá? Hát, én sem tudom. Talán az asztrociták és a neuronok nem értenek egyet, vagy talán az idegtudomány bonyolult. Az esetek bármelyikében szeretnék felülvizsgálni az asztrocitákat, mert az együttműködésük a 40% -ot képviseli forgalom glutamát, ami azt jelenti a glutamát nagy részét ezek a gliáiis sejtek nyerik ki .
Vannak más prekurzorok és egyéb utak is, amelyeken keresztül az extracelluláris térben felszabaduló glutamát visszanyerik. Például vannak olyan neuronok, amelyek egy specifikus glutamát transzporter -EAAT1 / 2-et tartalmaznak, amelyek közvetlenül a glutamátot visszanyerik a neuronba, és lehetővé teszik az excitatív jel végét. A glutamát szintézisének és anyagcseréjének további tanulmányozásához javaslom az irodalom olvasását.
A glutamát receptorok
Mint gyakran tanítunk, minden neurotranszmitternek van receptorai a posztszinaptikus sejtben . A sejtmembránban elhelyezkedő receptorok olyan fehérjék, amelyekhez egy neurotranszmitter, hormon, neuropeptid stb. Kötődik, hogy számos olyan változást eredményezzen a sejt sejtanyagcseréjében, amelyben a receptor található. Az idegsejtekben általában a receptorokat helyezzük a posztszinaptikus sejtekbe, bár ez nem feltétlenül igaz a valóságban.
Azt is tanítják az első fajban, hogy kétféle fő receptor van: ionotropikus és metabotróp. Az ionotrópok azok, amelyekben a liganduk kötve van - a receptor "kulcs" -ja csatornákat nyit, amelyek lehetővé teszik az ionok áteresztését a sejtbe. A metabotrópok viszont, amikor a ligandum kötve van, a második hírvivõk által okozott változásokat okoz a sejtben. Ebben a vizsgálatban a glutamát ionotrop receptorainak fő típusairól fogok beszélni, bár a metabotropikus receptorok ismeretére vonatkozó bibliográfia tanulmányozását javaslom. Itt idézem a fő ionotróp receptorokat:
- NMDA vevő.
- AMPA vevő.
- Kainado vevő.
Az NMDA és AMPA receptorok és szoros kapcsolatuk
Úgy véljük, hogy mindkét receptor típus négy makromolekula, melyeket négy transzmembrán domén képez, vagyis négy alegységből állnak, amelyek áthaladnak a sejtmembrán lipid kettős rétegénél, és mindkettő glutamát receptor, amely megnyitja a pozitív töltésű kationcsatornákat. De mégis, ezek jelentősen különböznek egymástól.
Az egyik különbség az a küszöb, amelyen aktiválódnak. Először is, az AMPA receptorok sokkal gyorsabban aktiválódnak; míg az NMDA receptorok nem aktiválódhatnak, amíg az neuron membránpotenciálja körülbelül -50 mV-nál van - egy neuron, ha inaktivált, általában körülbelül -70 mV. Másodszor, a lépcsős kationok minden esetben eltérőek lesznek. Az AMPA receptorok sokkal nagyobb membránpotenciálokat érnek el, mint az NMDA receptorok, amelyek sokkal szerényebbek. Viszonzásul az NMDA vevők időben sokkal tartósabb aktiválást érnek el, mint az AMPA. ezért az AMPA aktivitása gyorsan aktiválódik, és erősebb ingerlési potenciálokat eredményez, de gyorsan deaktiválódnak . Az NMDA aktivitása pedig lassan aktiválódik, de sikeresen megtartják az izgalmas potenciálokat, amelyeket sokkal hosszabb ideig hoznak létre.
Hogy jobban megértsük, képzeljük el, hogy katonák vagyunk és fegyvereink a különböző vevőket képviselik. Képzeld el, hogy az extracelluláris tér árok. Kétfajta fegyverünk van: revolver és gránát. A gránátok egyszerűek és gyorsan használhatók: eltávolítja a gyűrűt, a szalagokat, és megvárja, hogy felrobbanjon. Rengeteg pusztító potenciállal rendelkeznek, de miután mindent eldobtunk, vége. A revolver egy olyan fegyver, amely elviszi a terhelés idejét, mert el kell távolítania a dobot és egyenként fel kell raknia a golyókat. De miután betöltöttük, hat lövésünk van, amivel egy ideig megmarhatunk, bár sokkal kevésbé potenciális, mint egy gránát. Az agy revolvereink az NMDA vevők és gránátok az AMPA-k.
A glutamát feleslegessége és veszélyei
Azt mondják, hogy a többletben semmi sem jó, és a glutamát esetében teljesül. majd megemlítjük azokat a kórképeket és neurológiai problémákat, amelyekben a glutamát feleslege kapcsolódik .
1. A glutamát analógok exotoxicitást okozhatnak
A glutamát-szerű gyógyszerek - vagyis ugyanolyan funkciójuk van, mint a glutamát - mint például az NMDA -, amelyhez az NMDA receptor tartozik a nevéhez - nagydózisú neurodegeneratív hatásokat okozhat a legsebezhetőbb agyterületeken mint például a hypothalamus íves magja. A neurodegenerációban alkalmazott mechanizmusok változatosak és különböző típusú glutamát receptorokat tartalmaznak.
2. Néhány neurotoxin, amelyet a táplálékunkban lenyelünk, neuronális halált okoz a felesleges glutamáton keresztül
Egyes állatok és növények különböző mérgek hatását a glutamát idegi útvonalain keresztül fejtik ki. Példaként említjük a Cycas Circinalis, egy mérgező növényt, amelyet a Guam csendes-óceáni szigetén találunk. Ez a méreg okozott nagy előfordulást az amyotrophiás laterális szklerózisban ezen a szigeten, ahol lakói naponta bevessék azt hinni, hogy jóindulatú.
3. A glutamát az iszkémia által okozott neuronális halálhoz járul hozzá
A glutamát a fő neurotranszmitter az akut agyi rendellenességekben, például a szívrohamban , szívmegállás, pre / perinatal hypoxia. Ezekben az esetekben, amikor oxigénhiány van az agyszövetben, az idegsejtek állandó depolarizációs állapotban maradnak; különféle biokémiai folyamatok miatt. Ez a glutamát végleges felszabadulását eredményezi a sejtekből, a glutamát receptorok későbbi aktiválásával. Az NMDA receptor különösen kalciummal átjárható más ionotrop receptorokhoz képest, és a felesleges kalcium neuronális halálhoz vezet. Ezért a glutamáterg receptorok hiperaktivitása idegi halálhoz vezet az intraneuronális kalcium növekedése miatt.
4. Epilepszia
A glutamát és az epilepszia közötti kapcsolat jól dokumentált. Úgy vélik, hogy az epilepsziás aktivitás különösen az AMPA receptorokhoz kötődik, bár az epilepszia előrehaladtával az NMDA receptorok fontosak.

A glutamát jó? A glutamát rossz?
Általában, amikor az ilyen típusú szöveget olvassuk, a molekulák humanizálása a "jó" vagy "rossz" címkézéssel végződik - ez egy név, amelyet antropomorfizmus, nagyon divatos a középkorban. A valóság messze van ezektől a egyszerű ítéletektől.
Egy olyan társadalomban, amelyben létrehoztuk az "egészség" fogalmát, a természet mechanizmusainak egy része kényelmetlenül késztethet minket. A probléma az, hogy a természet nem érti az "egészséget". Ezt a gyógyszert, a gyógyszeriparot és a pszichológiát hoztuk létre. Ez egy társadalmi koncepció, és mint bármely társadalmi koncepció, a társadalmak előrehaladásának függvénye, akár emberi, akár tudományos. Az eredmények azt mutatják, hogy a glutamát számos betegséghez kapcsolódik mint például az Alzheimer-kór vagy a skizofrénia.Ez nem gonosz szem az evolúciónak az ember számára, inkább egy olyan fogalom biokémiai eltérése, amelyet a természet még mindig nem ért: az emberi társadalom a 21. században.
És mint mindig, miért tanulmányozta ezt? Ebben az esetben azt hiszem, a válasz nagyon világos. Mivel a glutamát szerepe különböző neurodegeneratív patológiákban, fontos - bár összetett - farmakológiai célt . Néhány példa ezekre a megbetegedésekre, noha e felülvizsgálat során nem beszéltünk róluk, mert úgy gondolom, hogy csak egy bejegyzést írhatok, az Alzheimer-kór és a skizofrénia. Szubjektív módon találom a skizofrénia új gyógyszereinek kutatását, amelyek alapvetően két okból fontosak: a betegség előfordulási gyakorisága és az egészségügyi költségek; és a jelenlegi antipszichotikumok káros hatásait, amelyek sok esetben gátolják a terápiás beilleszkedést.
A szöveg szerkesztette és szerkesztette Frederic Muniente PeixBibliográfiai hivatkozások:
könyvek:
- Siegel, G. (2006). Alapvető neurokémia. Amszterdam: Elsevier.
cikkek:
- Citri, A. & Malenka, R. (2007). Synaptic Plasticity: többféle formája, funkciói és mechanizmusai, Neuropsychopharmacology, 33 (1), 18-41. //dx.doi.org/10.1038/sj.npp.1301559
- Hardingham, G. & Bading, H. (2010). Synaptic vs. extraszinaptikus NMDA receptor jelátvitel: a neurodegeneratív rendellenességekre gyakorolt hatások. Nature Reviews, Neuroscience, 11 (10), 682-696. //dx.doi.org/10.1038/nrn2911
- Hardingham, G. & Bading, H. (2010). Synaptic vs. extraszinaptikus NMDA receptor jelátvitel: a neurodegeneratív rendellenességekre gyakorolt hatások. Nature Reviews, Neuroscience, 11 (10), 682-696. //dx.doi.org/10.1038/nrn2911
- Kerchner, G. & Nicoll, R. (2008). Csendes szinapszisok és a posztszinaptikus mechanizmus kialakulása az LTP számára. Nature Reviews, Neuroscience, 9 (11), 813-825. //dx.doi.org/10.1038/nrn2501
- Papouin, T. & Oliet, S. (2014). Az extraszinaptikus NMDA receptorok szervezése, ellenőrzése és funkciói. A Royal Society B: Biological Sciences, 369 (1654), 20130601-20130601. //dx.doi.org/10.1098/rstb.2013.0601